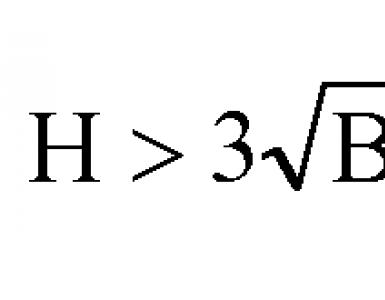Перегонка нефти. Нефтепродукты и их применение
Нашедших по-настоящему масштабное применение в технике только в XX веке, уходит, тем не менее, своими корнями в XVIII век. Век, когда о самом существовании кислорода и азота, не говоря уже об аргоне, научное сообщество и не подозревало. Воздух считался самостоятельным элементом, не подлежащим разделению на составляющие. Характер же горения тех или иных веществ, по господствовавшим тогда представлениям, определялся содержанием в них горючего компонента – флогистона. Чем больше в материале флогистона, тем он более горюч, и тем больше теплоты при высвобождении порождает.
Основы для более адекватного описания реальности заложили шведский химик Карл Шееле и его английский коллега Джозеф Пристли, которые, разделяя те или иные сложные соединения нагреванием, получили «горючий воздух», в котором пламя свечи горело куда ярче обычного. Шееле пошел еще дальше: он показал, что при сгорании веществ в изолированном сосуде количество воздуха уменьшается примерно на двадцать процентов, при этом в оставшемся воздухе горение невозможно. Однако приверженность теории флогистона вынуждала этих выдающихся ученых придумывать те или иные объяснения очевидным фактам в рамках устоявшейся догмы. Первым, кто, проведя серию опытов, предложил новую теорию горения, заявив, что воздух состоит из двух частей – горючей (кислород) и инертной (азот), – а вещество, сгорая, соединяется с кислородом, связывая его, был Лавуазье. Путем точных взвешиваний он установил, что масса продуктов горения всегда больше массы исходного вещества. В то же время масса запаянной колбы, в которой он сжигал те или иные реагенты не изменялась. В совокупности с установленным Шееле фактом уменьшения количества воздуха в процессе горения, Лавуазье и сделал вывод о том, что реакционноспособная часть воздуха связывается с исходным веществом, образуя продукты горения. Так были открыты кислород и азот.
Между тем прошло много лет, прежде чем эти газы смогли использовать в промышленных масштабах. На протяжении первых двух третей XIX века кислород получали в очень незначительных количествах лабораторными методами, поэтому ни о каком его широком применении речь не шла. Казалось бы, парадокс: атмосфера – целый океан кислорода и азота, осталось только найти способ разделить эти два газа, и проблема их получения решена. В то же время наиболее естественный способ разделения воздуха на кислород и азот – за счет разницы температур кипения, долгое время оставался недоступным. Прежде всего, в силу необходимости глубокого охлаждения воздуха. Вообще одно время азот и кислород считали «постоянными» газами, то есть газами, которые невозможно подвергнуть сжижению. Хотя, конечно, это отражало только отсутствие необходимых методов и технологий, а не какую-то принципиальную особенность данных газов.
Таким образом, одним из основных препятствий на пути промышленного получения атмосферных газов в чистом виде было несовершенство техники охлаждения. Одними из первых преодолеть данный барьер попытались польские физики Ольшевский и Врублевский (Краковский университет) параллельно с Джеймсом Дьюаром (Великобритания), применившие каскадный принцип охлаждения для сжижения кислорода и азота. Позднее с помощью этой же схемы Каммерлинг-Оннес (Нидерланды) получил и жидкий воздух. Суть метода состоит в последовательном понижении температуры при помощи нескольких рефрижераторов компрессионного типа с разными рабочими веществами.
Принцип действия каскадного процесса можно проследить с помощью рис. 1.
Сначала газ, выбранный в качестве охлаждающего агента, сжижают при комнатной температуре путем сильного сжатия с помощью компрессора. Тепло, выделяющееся при сжатии, отводится системой водяного охлаждения. Сжиженный газ подается в испаритель с более низким давлением, где кипит, отбирая теплоту, поступая затем в компрессор, где вновь сжижается. При этом испаритель первой ступени является одновременно охлаждающей ванной для сжиженного хдадагента второй ступени. Естественно, что для каждой ступени подбирают хладагент, температура кипения которого соответствует требуемым уровням охлаждения.
Рис. 1. Парокомпрессионный рефрижератор: 1 – компрессор; 2 – вода; 3 – бак системы охлаждения; 4 – дроссель; 5 – жидкость; 6 – испаритель (криостат)
Каскадный процесс сыграл важную роль в истории получения технических газов, показав принципиальную сжижаемость воздуха. Однако в дальнейшем он уступил место более совершенным технологическим схемам.
Метод Линде, предложенный этим немецким физиком в 1895 г. основан на эффекте Джоуля-Томпсона, который заключается в изменении температуры газа при расширении его через какое-либо гидродинамическое сопротивление (дросселирование). Дело в том, что внутренняя энергия реальных газов состоит из потенциальной энергии притяжения между частицами и кинетической энергией их хаотического движения. При расширении газа в условиях отсутствия энергообмена с внешней средой его потенциальная энергия взаимодействия молекул увеличивается, так как увеличивается расстояние между ними. Рост потенциальной энергии, вследствие «растаскивания» молекул на большее расстояние друг от друга, компенсируется уменьшением их кинетической энергии (энергии теплового движения), а следовательно, и температуры. Правда подобный эффект наблюдается только до определенного температурного порога, выше которого он изменяет знак: теперь при расширении газ нагревается. В этом случае просто меняет знак сама потенциальная энергия. Если раньше (до определенной температуры) она определялась силами притяжения, то теперь превалирующими являются силы отталкивания. И расширение (наоборот) придает дополнительный импульс тепловому движению молекул. Подобный «обращенный» эффект Джоуля-Томпсона при нормальных температурах характерен для водорода.
Впрочем, воздух охлаждается путем дросселирования на достаточно большом температурном интервале, что и позволило применить это его свойство в цикле Линде. В нем воздух сжимается компрессором до давления 200 атмосфер, теплоту сжатия отдает в теплообменнике и истекает через дроссельный клапан, при этом расширяясь и охлаждаясь. Охлажденный воздух протекает через тот же теплообменник, но с другой стороны, отбирая тепло у новой порции сжатого газа, после чего сам поступает на сжатие. Циркулируя таким образом достаточно долгое время, воздух охлаждается до такой температуры, что при дросселировании часть его начинает сжижаться. Впрочем, заслуга Линде состояла не только в том, что он смог поставить на промышленные рельсы сжижение воздуха, но в первую очередь в том, что он разделил сжиженный воздух, получив азот и кислород высокой степени очистки.
Для этого он применил двойную ректификацию полученного жидкого воздуха, так как простая перегонка не давала продукцию нужной чистоты. Несмотря на то, что температура кипения кислорода (-183 °С) выше температуры кипения азота (-196 °С) на тринадцать градусов, полностью разделить эти газы простым испарение азота не удавалось.
Сама идея ректификационной колонны состоит во встречном движении жидкости, обогащенной низкокипящим компонентом (в нашем случае азотом), навстречу парам газовой смеси, обогащенной высококипящим компонентом (кислородом). Жидкость подается сверху колонны, газовая смесь испаряется из ее нижней части.
Для увеличения поверхности контакта фаз применяют так называемые ректификационные тарелки. Соприкасаясь с ними, газ частично конденсируется, а жидкость частично испаряется. При этом в жидкое состояние переходит в основном высококипящая часть газа, а испаряется низкокипящая часть жидкости. В результате подобного обмена восходящий поток смеси газов обогащается низкокипящим компонентом, а нисходящий поток жидкости – высококипящим. В обычных ректификационных колоннах для создания обратного потока жидкости часть полученного на выходе из колонны низкокипящего компонента конденсируют и направляют назад.
Проблема в том, что жидкий воздух не удается разделить «с наскока». Применяя даже самые эффективные ректификационные колонны, мы можем получить на выходе достаточно чистый азот, но внизу колонны будет оставаться смесь азота с кислородом, хотя и обогащенная последним по сравнению с первоначальным составом воздуха.
Поэтому-то Линде и предложил схему двойной перегонки. Вкратце опишем происходящие в них процессы (рис. 2).
- 1) В первую (нижнюю) ректификационную колонну подается сжиженный воздух, который в процессе перегонки разделяется на почти чистый азот и азотно-кислородную смесь.
- 2) Азот конденсируется в верхней части первой колонны, откуда отбирается, направляясь затем в жидком виде в верхнюю часть второй (верхней) колонны, формируя поток жидкости, стекающей вниз.
- 3) Азотно-кислородная смесь подается в среднюю часть второй колонны. Так как процесс непрерывен, там ее уже поджидают, с одной стороны, поток газов из испарителя, обогащенный кислородом, а с другой – стекающая сверху жидкость, обогащенная азотом.
- 4) Попав под такой «перекрестный огонь», азотно-кислородная смесь начинает разделяться в соответствии с ранее описанными принципами. Вверх с газами в итоге уходит чистый азот, а внизу собирается чистый кислород.
Изящность предложенной схемы состоит, кроме всего прочего, в том, что испаритель второй колонны является одновременно конденсатором для первой. Это позволяет существенно сократить расход энергии. Между тем необходимый температурный режим обеспечивается разностью давлений в двух колоннах и поддерживается автоматически.
Параллельно с Линде над разделением воздуха работах французский ученый Клод. При этом для предварительного сжижения он использовал не дросселирование, а детандеры – машины, в которых газ, расширяясь, совершал работу и охлаждался. Данная технология оказалась менее эффективной, нежели предложенная Линде, прежде всего, из-за сложностей работы механических деталей при низкой температуре. Между тем к началу тридцатых годов в общих чертах был разработан турбодетандер, в котором воздух (или любой другой газ), расширяясь, вращает лопасти турбины, за счет чего охлаждается с последующим сжижением. Подобные устройства даже начали частично применяться в промышленном производстве, но обладали достаточно низким КПД. Прорыв в использовании турбодетандеров обеспечил П. Л. Капица, предложивший, казалось бы, очевидную идею, до которой, тем не менее, никто до него не додумался. Ранее для сжижения газов использовалась турбина, близкая по характеристикам к паровой. Капица же обратил внимание на то, что холодный сжатый воздух, работающий в ней, по свойствам ближе к жидкости, чем к пару. Это побудило его взять за прототип для нового турбодетандера водяную турбину: "...правильно выбранный тип турбодетандера будет как бы компромиссом между водяной и паровой турбиной " – считал Капица. Это действительно резко повысило КПД сжижения газов, так что теперь именно турбодетандер, разработанный Капицей, является основой получения жидкого воздуха. Последующее же его разделение идет по схеме, предложенной еще Линде.

Рис. 2. Аппарат двукратной ректификации: 1, 2 – ректификат колонны; 3 – конденсатор-испаритель
Впрочем, воздух состоит не только из азота и кислорода. Он содержит в небольших количествах такие инертные газы, как аргон, неон, криптон и ксенон. Неон, как легкокипящий компонент, собирается под крышкой второй ректификационной колонны вместе с гелием. Неонно-гелиевую смесь очищают от азота в противоточном дефлегматоре. А сам неон извлекают из нее адсорбционным методом. Криптон и ксенон, как высококипящие компоненты, уходят вниз колонны вместе с кислородом. Смесь кислород-криптон-ксенон разделяется в дополнительной колонне на чистый кислород и так называемый «первичный концентрат», где содержание инертных газов выше, чем в первоначальной смеси. И уже из первичного концентрата путем адсорбции выделяют криптон и ксенон.
Сложнее с аргоном. Его температура кипения ниже, чем у кислорода, но выше, нежели у азота. Поэтому часть его выходит с кислородом, а другая часть – с азотом. Чтобы предотвратить подобное развитие событий, из средней части колонны отбирают некоторую долю находящейся там смеси, направляя ее в дополнительную колонну разделения, откуда освобожденная от аргона кислородно-азотная смесь возвращается обратно, а концентрат аргона поступает на дальнейшее очищение.
Отметим, что на сегодняшний день, кроме криогенного, существуют и другие способы разделения газов.
Так, например, адсорбционный способ характеризуется низкой себестоимостью, легкостью управления производственным процессом и достаточно высокой степенью чистоты получаемых газов. В основу данного способа положена способность некоторых веществ специфически (преимущественно) поглощать те или иные газы. При получении азота, воздух под давлением подается в адсорбер, содержащий углеродные молекулярные сита (рис. 3). В результате кислород поглощается адсорбентом, а на выходе получаем азот. В то же время объем кислорода, который может поглотить адсорбент, ограничен, поэтому необходимо постоянно проводить регенерацию молекулярных сит. Обычно это достигается сбросом давления: кислород испаряется с поверхности адсорбента, и последний готов к разделению новой партии воздуха.
Для получения кислорода используют тот факт, что азот адсорбируется на алюмосиликатных ситах быстрее, чем кислород. Поэтому, пропуская воздух через адсорбер с алюмосиликатным наполнением, на выходе получаем кислород чистотой до 95 %.

Рис. 3. Адсорбционное разделение газов:
а) схема получения азота из воздуха адсорбционным методом;
б) установка для адсорбционного разделения газов
Мембранный способ разделения воздуха – еще один метод получения газов из атмосферы. Он основан на том, что составляющие воздуха с различной скоростью проходят через газопроницаемые мембраны, обычно полимерные (рис. 4). Воздух при этом, подается под давлением в мембранный модуль, состоящий из множества полых полимерных волокон с нанесенным на них газоразделительным слоем. Молекулы кислорода и аргона «продавливаются» сквозь мембрану наружу, а в волокнах остается обогащенная азотом газовая смесь. Последовательное фильтрование воздуха сквозь несколько мембранных модулей позволяет получить достаточно чистый азот (до 99,9 %).


Рис. 4. Мембранное разделение газов:
а) мембраны – полые полимерные волокна;
б) установка для мембранного разделения
И мембранный и адсорбционный способы разделения воздуха, позволяя получить относительно чистый азот, не могут, тем не менее, похвастаться выделением кислорода с нужной для технических целей чистотой, не говоря уже об аргоне и других газах. Поэтому основным способом разделения газов на сегодняшний день остается метод криогенной ректификации, позволяющий получать конечные продукты, практически свободные от примесей.
Под термином фракционная перегонка следует понимать последовательное многократное повторение процесса испарения и конденсации.
Ректификация - непрерывное многократное повторение процесса испарения и конденсации.
Фракционная перегонка служит для разделения однородной смеси жидкостей, кипящих при различной температуре и не образующих друг с другом постоянно кипящих смесей. В основе всякой дробной перегонки лежит закон фазового равновесия в системе жидкость--пар, открытый Д. П. Коноваловым: ?пар обогащен тем компонентом, прибавление которого к жидкости понижает ее температуру кипения? (т.е. более легкокипящим) и служит для более совершенного разделения смеси, особенно в случае малой разницы температур кипения ее компонентов.
Вследствие того, что поверхность соприкосновения пара и жидкости в колонне велика, облегчается теплообмен и улучшается разделение фаз (пара и жидкость). Благодаря этому жидкая фаза, возвращаясь в перегонную колбу, обогащается менее летучим компонентом, а газовая фаза, поступающая вверх, обогащается более летучим компонентом.
Из диаграммы фазового равновесия видно что, паровая фаза при любой температуре кипения содержит большее количество низкокипящего компонента, чем жидкая фаза; при этом каждой температуре кипения соответствуют строго определенные составы жидкости и пара.
Таким образом, пар, образующийся из кипящей бинарной смеси, всегда содержит оба компонента, но обогащен более летучим из них (состав M1). При полной конденсации такого пара получается жидкость с тем же составом, что и пар. При вторичной перегонке этой жидкости образуется пар (состав M2), еще более обогащенный легкокипящим компонентом. Следовательно, в результате многократного повторения условий фазового равновесия (перегонки) для каждой первой фракции можно в конечном счете получить в первой фракции от последней перегонки низкокипящей компонент смеси, не содержащий другого компонента. Соответственно, последняя фракция будет состоять из чистого высококипящего компонента первоначальной смеси. В этом по существу и заключается принцип разделения дробной перегонки.
В качестве простых перегонных колон в лаборатории используют различного типа дефлегматоры (рис.46), эффективность которых тем выше, чем больше площадь их поверхности.

Действие дефлегматоров состоит в том, что в них при неполном охлаждении пара кипящего раствора происходит частичная конденсация пара более высококипящей жидкости. Образовавшийся промежуточный конденсат называют флегмой.
Флегма стекает обратно в реакционную колбу, а пар обогащается компонентом с более низкой температурой кипения и попадает в холодильник, где подвергается уже полной конденсации.
Дефлегматоры способствуют выделению порции конденсата с узким интервалом температуры кипения порядка 1-2oС.
В случае фракционной перегонки смесь разгоняют в приборе (рис. 47), состоящем из перегонной колбы с дефлегматором, термометра, холодильника, аллонжа и приемника.
После того как прибор собран и установлен, загружают рабочую смесь.

Рис. 47.
Дистиллят должен поступать в приемник со скоростью 30-40 капель в минуту. При достижении верхнего предела температурного интервала первой фракции меняют приемник. Не прекращая нагревания, продолжают собирать следующую фракцию во второй приемник. Затем приемник меняют на третий. Перегонку прекращают, когда в перегонной колбе остается 2-3 мл жидкости.
Для лучшего разделения смеси веществ проводят вторичную разгонку. В перегонную колбу помещают первую фракцию и перегоняют ее в прежних температурных пределах. Когда температура отходящих паров достигнет верхней границы первого температурного интервала, перегонку прекращают, и прибор охлаждают. В перегонную колбу добавляют среднюю фракцию от первой перегонки и вновь начинают разгонку, как описано выше. По окончании перегонки средней фракции к остатку приливают третью фракцию и продолжают разгонку, собирая фракции в 2-й и 3-й приемники. При многократном повторении разгонки средняя фракция значительно уменьшается, разделяясь на первую и третью фракции. При этом происходит сужение температурных интервалов крайних фракций. Таким способом удается достаточно хорошо разделить смесь компонентов, имеющих очень близкий температурный интервал кипения.
Азеотропная смесь -- смесь двух или более жидкостей, состав которой не меняется при кипении, то есть смесь с равенством составов равновесных жидкой и паровой фаз.
Например, азеотропная смесь воды и этилового спирта содержит 95,57% C2H5OH и кипит при температуре 78,15 °C. Этим объясняется принятая промышленная концентрация этилового спирта 96%: это азеотропная смесь и дальнейшей перегонкой её нельзя разделить на фракции. Температура кипения для азеотропной смеси может быть как меньше (положительные азеотропы), так и больше (отрицательные азеотропы) температуры кипения низкокипящего компонента.
При изменении давления изменяется не только температура кипения, но и состав азеотропной смеси, этим они отличаются от чистых жидкостей.
Для разделения азеотропных смесей используют различные технологии:
Удаление одного из компонентов за счёт адсорбции на твёрдом пористом материале.
Разделение на пористых мембранах
Первапорация на непористых мембранах
Перегонка при давлении, отличном от атмосферного, в частности - под вакуумом, см. выше.
Перегонка с дополнительным компонентом, с созданием тройного (или более) азеотропа
Фазовая диаграмма двухкомпонентного положительного азеотропа.
перегонка давление шлиф

Слово азеотропа происходит от греческого слова жЭейн (кипение) и фсьрпт (государство) в сочетании с префиксом б-(нет), чтобы дать общий смысл ", никаких изменений при кипячении".
Азеотропная перегонка
Многие вещества, взятые в определенном соотношении, образуют друг с другом азеотропные смеси. К числу известных азеотропных смесей принадлежат, например, 96% этиловый спирт (водн.) -- т. кип. 78,15 °С -- минимальная температура кипения; концентрированная бромоводородная кислота, имеющая постоянную температуру кипения 126 °С -- максимальная температура кипения по сравнению с обоими компонентами смеси (бромоводород и вода).
При нагревании смеси двух веществ, образующих азеотроп с максимальной температурой кипения, сначала отгоняется компонент, присутствующий в избытке по отношению к составу смеси азеотропа. После этого отгоняется азеотроп с максимальной температурой кипения (имеющий минимальную упругость паров). При перегонке смеси, образующей азеотроп с минимальной температурой кипения, сначала отгоняется азеотропная смесь, а потом компонент, имеющийся в избытке. Известно более 3000 двойных азеотропных смесей с минимумом температуры кипения и только около 250 с максимумом (как правило, это гомогенные смеси сильно полярного характера)***.
Очень большое значение в практике имеет азеотропная сушка. Для этого к высушиваемому веществу добавляют соединение, образующее с водой азеотропную смесь и, желательно, не смешивающееся с водой на холоду (например, бензол). Затем смесь нагревают, отгон конденсируют в нисходящем холодильнике и собирают в градуированную емкость. Вода, образующая с бензолом азеотропную смесь (т. кип. смеси 60 °С, воды --100 °С, бензола -- 80 °С), разделяется в приемнике на два слоя. Таким способом можно не только высушить вещество, контролируя момент окончания выделения воды, но и наблюдать за течением реакций, при которых выделяется вода, а также отгонкой воды смещать равновесные реакции в желаемом направлении.
Известные азеотропные смеси приведены в кн.: Гордон А., Форд Р. Спутник химика. М., Мир, 1976. 28
Наиболее часто для отделения воды при азеотропной сушке используют бензол, изомерные ксилолы, толуол, хлороформ и тетрахлорид углерода. При этом не надо забывать, что CHCl3 и CCl4 тяжелее воды.
Перегонка, или дистилляция, - процесс разделения бинарных и многокомпонентных жидких смесей на отдельные компоненты. При этом можно рассматривать в отдельности два процесса: переход жидкости в парообразное состояние и конденсацию пара.
Жидкость закипает, когда давление ее насыщенного пара становится равным внешнему давлению. Температура кипения жидкости изменяется с изменением давления. При перегонке чистого индивидуального вещества температура кипения при определенном давлении постоянна, так как состав жидкости и образующегося пара одинаков. В случае перегонки смеси жидких веществ, компоненты которых смешиваются друг с другом в любом соотношении, состав пара и жидкости все время изменяется в результате обогащения газовой фазы более летучим компонентом.
Пар, обогащенный более летучим компонентом, конденсируется. В результате получается жидкость (дистиллят) с тем же составом, что и пар. При перегонке дистиллята вначале образуется пар, еще более обогащенный легкокипящим компонентом.
В результате подобной многократной перегонки можно практически разделить смесь на чистые компоненты. В этом заключается сущность метода разделения смеси жидких веществ путем дробной (фракционной) перегонки. Разделение смеси веществ методом дробной перегонки тем легче, чем больше разница между составом жидкости и составом пара. Однако методом дробной перегонки нельзя разделить азеотропные (нераздельно кипящие) смеси.
Дробная перегонка - чрезвычайно длительный процесс даже для разделения смеси, состоящей из двух веществ. При большем числе компонентов возникают еще большие трудности, которые могут быть устранены перегонкой в колонке для точного фракционирования. В результате этого процесса образуется ряд отграниченных друг от друга фракций, кипящих в узких температурных пределах.
Перегонку можно проводить не только при атмосферном, но и при повышенном и уменьшенном давлении. Перегонка при уменьшенном давлении применяется для разделения компонентов высококипящих жидкостей, которые при температуре кипения под атмосферным давлением разлагаются или изменяются. Желаемая температура кипения достигается путем соответственного уменьшения остаточного давления.
Для очистки или разделения веществ, особенно термически малостойких, мало растворимых в воде, или легко отделяющихся от воды, часто используют перегонку с насыщенным или перегретым водяным паром.
Простая перегонка при атмосферном давлении
Простая перегонка сводится к частичному испарению кипящей жидкой смеси, полному отводу и конденсации образовавшихся при этом паров. Как правило, простую перегонку применяют для разделения термически устойчивых жидких веществ, сильно отличающихся по своим температурам кипения; для отделения жидкости от растворенных в ней твердых веществ; для концентрирования растворов; для очистки сжиженных газов и т. п.
Простейший прибор для перегонки при атмосферном давлении состоит из колбы Вюрца, к горлу которой припаяна трубка для отвода паров кипящей жидкости в холодильник, или из отдельной колбы, снабженной насадкой Вюрца, термометром, нисходящим холодильником, алонжем и приемником (рис. 156). В качестве перегонной колбы можно использовать круглодонную, остроконечную или грушевидную колбы. Колбу Вюрца или отдельную перегонную колбу выбирают такой вместимости, чтобы перегоняемая жидкость занимала не более 2/3 объема. Для перегонки высококипящих жидкостей следует пользоваться короткогорлыми колбами. Небольшие объемы жидкостей лучше перегонять из остроконечных колб, оттянутая форма которых позволяет вести отгонку до минимального остатка. Наиболее пригодна грушевидная форма перегонной колбы, обеспечивающая почти постоянную поверхность испарения при уменьшении содержимого колбы.

Стеклянную насадку Вюрца выбирают так, чтобы номер КШ керна соответствовал номеру КШ муфты перегонной колбы. Для конденсации пара применяют обычный нисходящий холодильник. Длина холодильника должна быть тем больше, чем ниже температура кипения жидкости.
Пары твердых при комнатной температуре веществ не должны охлаждаться в холодильнике до температуры затвердевания. Во избежание этого рекомендуется холодильник периодически прогревать теплой (горячей) водой.
При перегонке жидкостей, кипящих выше 150 °С, применяют только воздушные холодильники. Жидкости, кипящие в пределах 200-300 °С, перегоняют без холодильника, функцию которого в этом случае может выполнять отводная трубка насадки перегонной колбы (рис. 157).
При перегонке низкокипящих веществ приемную колбу помещают в ледяную или охладительную баню.
Перегонку веществ вредных для здоровья (сероуглерод, тионилхлорид и др.), следует выполнять в вытяжном шкафу.
Устанавливать термометр в горло перегонной колбы нужно так, чтобы ртутный шарик его находился не менее чем на 5 мм ниже нижнего края отверстия отводной трубки в шейке колбы Вюрца или дистилляционной насадки. В этом случае термометр хорошо омывается парами жидкости, что обеспечивает правильное измерение температуры кипения. На конце шарика термометра должна удерживаться капля конденсата; ее отсутствие указывает на то, что пар в колбе перегрет и, следовательно, регистрируемая температура не соответствует истинной температуре кипения.

В качестве приемника дистиллята может служить коническая склянка или круглодонная колба. Приемник присоединяют к холодильнику с помощью алонжа с отводной трубкой, служащей для отвода не сконденсировавшихся вредных или опасных паров газов в безопасное место или в промывную склянку с соответствующим поглотителем (нейтрализатором).
Если дистиллят чувствителен к влаге или диоксиду углерода, к отводной трубке алонжа присоединяют хлоркальциевую трубку, заполненную СаСl2, натронной известью или аскаритом. Если перегоняемое вещество чувствительно к кислороду, то перегонку ведут в токе сухого азота. При этом приемную колбу следует присоединять к поглотительной склянке, заполненной раствором, поглощающим кислород.
Когда установка собрана, в колбу вливают перегоняемую жидкость и для равномерного кипения вносят кусочки необожженного фарфора, кирпича, а также заплавленные с одной стороны стеклянные капилляры, которые помещают в колбу открытым концом к низу. Сильный перегрев может сопровождаться «взрывным» кипением, разбрызгиванием и перебрасыванием перегоняемой жидкости.
При длительном кипячении все количество адсорбированного «кипелкой» воздуха может оказаться израсходованным, и жидкость начинает кипеть неравномерно. Тогда необходимо повторно ввести «кипелки» (или капилляры), предварительно охладив жидкость ниже температуры кипения, иначе жидкость может внезапно бурно вскипеть.
Перегонную колбу нагревают газовой горелкой через асбестовую сетку, на закрытой электрической плитке или с помощью колбонагревателя, на водяной, воздушной, масляной или металлической бане. Нагревание на бане обеспечивает равномерность нагрева, предотвращает перегревы и связанные с ними нарушения процесса кипения. Температура бани не должна превышать температуру кипения перегоняемого вещества больше чем на 20-30 °С.
Нагревание проводят так, чтобы перегонка проходила не слишком быстро. При слишком интенсивном кипении в результате перегрева паров в колбе создается повышенное давление, и измеряемая температура не соответствует температуре кипения данной фракции при атмосферном давлении. Скорость перегонки считается нормальной, если из холодильника стекает 30-35 капель конденсата в минуту.
При перегонке индивидуальных веществ температура кипения постоянна в течение всего процесса, лишь к концу перегонки она может подняться на несколько градусов. Непрерывное повышение температуры кипения свидетельствует о том, что отгоняется смесь веществ.
Для увеличения эффективности разделения смеси, когда простая перегонка не позволяет добиться нужных результатов, пользуются перегонной колбой с дефлегматором. Дефлегматоры часто называют фракционирующими насадками; некоторые из них послужили прообразом современных ректификационных колонок.
В дефлегматоре за счет охлаждения наружным воздухом часть паров перегоняемой смеси конденсируется, причем конденсат (флегма) содержит преимущественно менее летучий компонент, а пары - более летучий.
Когда стекающий конденсат соприкасается с поднимающимися вверх парами кипящей жидкости, между ними происходит взаимодействие, приводящее к дополнительной конденсации менее летучего компонента и испарению легколетучего.
Для разделения смеси жидкостей, имеющих относительно близкие температуры кипения, обычные дефлегматоры практически малоэффективны. В практике для повышения эффективности простых и вакуумных перегонок используют дефлегматоры различных конструкций и колбы Фаворского и Арбузова (рис. 158).
При простой перегонке под атмосферным давлением боковая горловина колбы Фаворского служит для загрузки перегоняемой жидкости, выгрузки остатка от перегонки, внесения «кипелок», пропускания тока инертного газа и установки термометра. При вакуумной перегонке, чтобы предотвратить бурное вскипание жидкости, в боковую горловину вставляют капиллярную трубку для перемешивания жидкости пузырьками воздуха или инертного газа.
Колба Арбузова представляет собой перегонную колбу, спаянную с шариковым дефлегматором. На дно каждого шара такого дефлегматора помещен стеклянный шарик, что значительно повышает разделительную способность дефлегматора.
Дробная перегонка
При простой перегонке нельзя добиться полного разделения смеси, а можно лишь выделить отдельные фракции, причем первая будет обогащена более летучим компонентом, а последняя - менее летучим. Средняя, промежуточная, фракция будет состоять из смеси низко- и высококипящих компонентов. При дробной перегонке процессы испарения и конденсации многократно повторяются; дистиллят каждый раз становится исходным материалом для следующего процесса. В результате концентрируется низкокипящий компонент.
Дробной перегонке предшествует пробная перегонка, в результате которой узнают величину всего интервала кипения смеси. Пусть этот интервал равен 90-135 °С. Предположим, что разделяемая смесь состоит из двух веществ с температурами кипения 90 и 135 °С. Интервал между температурами кипения делят на три равные части. При первичной перегонке собирают фракции: I - в пределах 90-105 °С, II - 105-120 °С и III - 120-135 °С. Фракцию I перегоняют вторично до тех пор, пока термометр не покажет 105 °С. При этой температуре перегонку прерывают и прибавляют к остатку в колбе фракцию II и снова доводят жидкость до кипения. То, что перегонится до 105 °С, собирают в тот же приемник. Когда температура достигнет 105°С, меняют приемник и отгоняют жидкость до 120 °C. Снова прерывают перегонку, прибавляют к остатку фракцию III, нагревают и, когда температура достигнет 120 °С, меняют приемник и собирают дистиллят, перегоняющийся при 120-125 °С. После вторичной разгонки оказывается, что количество вещества в I и III фракциях увеличилось, а во II фракции значительно уменьшилось.
Нередко дробную перегонку целесообразно проводить при уменьшенном давлении, особенно в тех случаях, когда компоненты смеси имеют близкие температуры кипения и относятся к разным классам соединений. Иногда различие в температурах кипения таких веществ в вакууме может быть значительно большим, чем при атмосферном давлении.
Ректификация в колонках
Ректификация - многократное испарение и конденсация - реализуется в колонках при противотоке пара и жидкости с частичным возвратом (флегмой) дистиллята при установившихся массо- и теплообмене. В ректификационных колонках в условиях известного температурного перепада по всей длине колонки создается последовательный ряд фазовых равновесий между конденсатом, стекающим обратно в перегонную колбу, и поднимающимся вверх паром. При этом высококипящий компонент частично конденсируется из паровой фазы, а низкокипящий - испаряется из флегмы.
Разделение компонентов на колонке должно происходить в условиях адиабатического процесса. Тепловые потери приводят к нарушению состояния равновесия, при этом пар конденсируется вдоль стенок колонки. Разделение протекает тем полнее, чем больше поверхность соприкосновения между флегмой и паром.
Для увеличения поверхности соприкосновения пара и флегмы в лабораторных условиях применяют так называемые на садочные колонки, представляющие собой стеклянные или кварцевые трубки с насыпной насадкой из одиночных стеклянных или проволочных витков. Поверхность соприкосновения пара и жидкости в колонке велика, поэтому облегчается теплообмен и улучшается разделение компонентов.
Флегма, возвращаясь в перегонную колбу, обогащается менее летучим компонентом, а газовая фаза, поступающая вверх, - более летучим.
Скорость установления равновесия фаз в колонке зависит от ее конструкции. За установлением равновесия в колонке обычно следят по показанию термометра. В момент заполнения колонки парами термометр показывает некоторую температуру, которая со временем понижается до определенного уровня. Достижение этого уровня означает, что установилось равновесие, т. е. пары максимально для данной колонки обогатились наиболее летучим компонентом.
Важный фактор точного фракционирования на колонке - флегмовое число, измеряемое долей конденсата, возвращаемого в колонку для орошения, т. е. конденсата, стекающего из головки колонки в ректифицирующую трубку с насадкой. Величину флегмового числа обычно регулируют при помощи, выходного крана по числу капель флегмовой жидкости и числу капель отбираемого дистиллята так, чтобы до тех пор, пока продукт получается в чистом виде, отбираемое в единицу времени количество его поддерживалось примерно постоянным. Однако, как только количество отгоняемого вещества уменьшается или температура кипения повышается, что указывает на начало отгонки более высококипящей составной части смеси, скорость отбора дистиллята следует сильно уменьшить.
Конденсация паров, прошедших через ректификационную колонку, и разделение конденсата на флегмовую жидкость, стекающую обратно из колонки в перегонную колбу, и отбираемые порции дистиллята, происходят в головке колонки. Если в головке задерживается только часть паров, конденсат которых идет на орошение колонки, а другая часть паров конденсируется в холодильнике и отбирается в виде фракции дистиллята, то такие головки называют головками частичной конденсации. В лабораторных колонках аналитического и препаративного назначения преимущественно применяются головки полной конденсации, в которых конденсируются все пары, а конденсат специальным устройством разделяется на флегмовую жидкость и дистиллят.
Во время перегонки одного компонента температура кипения держится постоянной, затем скачкообразно повышается вследствие появления в дистилляте другого компонента и опять держится на постоянном уровне, соответствующем температуре кипения этого компонента. Во время «скачка» температуры получаются различные количества промежуточных фракций. Колонка считается тем эффективней, чем меньше количество промежуточных фракций.
Рабочая мощность колонки оценивается количеством паров и жидкостей, проходящих противотоком через колонку, не вызывая ее «захлебывания», т. е. заполнения центральной трубки избытком флегмы. Каждая колонка имеет некоторую оптимальную скорость перегонки, при которой она работает наиболее эффективно. При выборе колонки следует учитывать также и то, что часть конденсата расходуется на орошение внутреннего пространства колонки. Эта неиспользованная часть продукта не отбирается в виде дистиллята. Количество перегоняемой жидкости должно быть по меньшей мере в 20 раз больше количества конденсата, орошающего колонку.
Сравнительную разделительную эффективность колонок для ректификации условно оценивают числом теоретических тарелок (ЧТТ). Другая величина, характеризующая эффективность ректификационной колонки - высота, эквивалентная одной теоретической тарелке (ВЭТТ), которая получается делением высоты колонки на число теоретических тарелок.
В лабораторной практике пользуются разнообразными типами перегонных колонок. Во многих лабораториях особенно широко используются колонки с насыпной насадкой из одиночных витков стеклянной спирали или обрезков металлической проволочной спирали. Один из вариантов подобных стеклянных колонок представлен на рис. 159.

Стеклянные детали для сборки лабораторных колонок точной ректификации при атмосферном и пониженном давлении с высотой ректифицирующей части 400 и 1100 мм выпускаются серийно. Общая длина центральной трубки с головкой полной конденсации 840 и 1620 мм. Объем перегоняемой жидкости 10-50 и 50-500 мл. Соединение деталей установки выполнено на нормальных взаимозаменяемых шлифах. Общий вид колонок, собранных из стеклянных деталей, представлен на рис. 160.
Ректификационная стационарная лабораторная установка РУТ предназначена для разделения различных веществ в непрерывном или периодическом процессе. На установке можно производить ректификацию как при уменьшенном, так и при атмосферном давлении. Установки выпускаются с.колонками тарельчатого типа трех типоразмеров РУТ-20, РУТ-25 и РУТ-55. Для разделения больших объемов органических веществ при атмосферном и пониженном давлении выпускается стационарная лабораторная установка с насадочной колонкой УПФ. ДЛЯ разделения нефтяных фракций углеводородных смесей и сложных смесей других органических соединений в лабораторных условиях изготовляется аппарат четкой ректификации АЧР-2.
В соответствии с конструкцией применяемой колонки в значительной степени меняется и техника перегонки. Однако имеются общие операции проведения перегонки на насадочных колонках, краткое описание которых приводим ниже.
Когда из стеклянных деталей собрана колонка (согласно прилагаемой инструкции), ее следует промыть и просушить. Для этого в колбу для перегонки помещают этиловый спирт, нагревают колбу при закрытом кране для отбора проб дистиллята и одновременно пускают воду, охлаждающую головку колонки. Затем устанавливают такой режим обогрева, чтобы число капель, падающих в колонку из головки в единицу времени, было в 2-2,5 раза меньше, чем число капель, падающих из колонки в колбу, а температура рубашки была на 5-10 °С ниже температуры кипения спирта. При этом колонка «захлебывается». В результате этого из насадки вытесняется воздух и вся она смачивается флегмой. Уменьшая нагрев перегонной колбы, дают стечь избытку флегмы в течение 15-20 мин, после чего, сохраняя установленный обогрев колонки, усиливают нагрев колбы, пока в головке вновь не соберется столб жидкости. Целесообразно держать колонку в состоянии «захлебывания» 5-10 мин и чтобы объем жидкости над насадкой составлял 10-25% объема насадки. «Захлебывание» повторяют 2-3 раза, затем устанавливают режим разгонки и заставляют колонку работать 30-60 мин при полном орошений, отбирают несколько раз по 0,5-1,0 мл дистиллята, чтобы промыть кран и отводные трубки, после чего выключают нагрев колбы. Когда вся флегма стечет из колонки, колбу отсоединяют, прокачивают через колонку сухой воздух с помощью водоструйного насоса, присоединяемого к отводной трубке головки, из которой на это время выпускают воду. После выполнения описанных операций колонка готова к работе.
Перегоняемое вещество помещают в колбу для перегонки. Если температуры кипения компонентов смеси не превышают 150 °С, перегонку предпочитают проводить при атмосферном давлении, при более высоких температурах - при пониженном: 133 Па (1 мм рт. ст.).
Перегонную колбу предпочтительнее всего нагревать на жидкостной бане с регулируемым обогревом. Включив нагрев перегонной колбы, устанавливают режим обогрева колонки, как было описано выше, и 2 раза дают колонке «захлебнуться». После этого устанавливают требуемый режим обогрева колбы и рубашки. При полном орошении колонку выдерживают около 1 ч для того, чтобы установилось равновесие фаз. Далее опытным путем устанавливают оптимальный режим работы колонки.
При работе с колонками, у которых отсутствует обогрев, режим работы определяется только скоростью испарения жидкости.
Отбор дистиллята можно проводить непрерывно и периодически. При непрерывном отборе слегка открывают кран для отбора дистиллята у головки полной конденсации так, чтобы установить заранее заданное флегмовое число (1:10, 1:20, 1:30).
Температуру измеряют при каждом отборе дистиллята.
Если в приемнике собирается индивидуальное вещество, признаком чего служит постоянство температуры паров в головке в течение некоторого времени, величину флегмового числа можно уменьшить, увеличивая скорость отбора дистиллята. При переходе от фракции к фракции флегмовое число вновь увеличивают, уменьшая скорость отбора дистиллята. Это называется «отжимом фракции».
При периодическом отборе дистиллята на 1-5 с полностью открывают кран для отбора дистиллята, спускают небольшое количество последнего в приемник и закрывают кран. Так как при этом удаляется часть легколетучего компонента, то равновесие в колонке нарушается, и температура пара в головке начинает увеличиваться. Когда кран вновь закрывают, в колонке постепенно устанавливается состояние равновесия, и температура пара при этом понижается. Когда температура установится, вновь отбирают пробу дистиллята. Температуру и объем дистиллята отсчитывают непосредственно в момент отбора очередной порции дистиллята.
При ректификации в вакууме головку колонки снабжают вакуум-приемником.
Перегонка в вакууме
Некоторые вещества не могут быть перегнаны при атмосферном давлении ввиду частичного или полного разложения их при температуре кипения. Такие вещества можно перегнать при условии, если давление в перегонной колбе будет понижено настолько, чтобы температура кипения вещества оказалась ниже температуры его разложения. Например, вещества, кипящие с разложением при 350 °С и 101 кПа (760 мм рт. ст.), можно перегнать без разложения при 160-210 °С и 1,33 кПа (10 мм рт. ст.) или при 100-130 °С и 1,33 Па (0,01 мм рт. ст.).
При вакуумной перегонке вещества в меньшей степени подвержены действию кислорода. В ряде случаев, как было указано выше, вакуумная перегонка способствует разделению азеотропных смесей.
Прибор для перегонки в вакууме (рис. 161) состоит из перегонной колбы, приспособления для ее нагрева, термометра, холодильника, приемника конденсата или приспособления для смены приемников, источника вакуума и приспособления для измерения и регулирования давления.

В качестве перегонной колбы могут быть использованы колбы Кляйзена, Фаворского и Арбузова, а также круглодонные или остродонные колбы на шлифах с дистилляционной насадкой или холодильником Кляйзена.
Форма и вместимость перегонной колбы определяются объемом и температурными пределами кипения перегоняемой жидкости. Объем последней не должен превышать 1/2 объема колбы. Высококипящие жидкости следует перегонять из колб с низкоприпаянной и широкой боковой отводной трубкой.
В центральное горло колбы Кляйзена или дистилляционной насадки Кляйзена для предупреждения «взрывного» вскипания вставляют тонкооттянутый стеклянный капилляр, доходящий почти до дна колбы. О пригодности капилляра судят, продувая через него воздух в пробирку с диэтиловым эфиром. Хороший, капилляр даже при небольшом избыточном давлении пропускает лишь мелкие отдельные пузырьки, образующие в жидкости тонкую цепочку. После подключения прибора к вакуум-насосу через жидкость должны проходить очень мелкие пузырьки газа (воздуха), обеспечивающие перемешивание перегоняемой жидкости и равномерность кипения.
В боковое горло перегонной колбы или насадки помещают термометр.
В случае пользования колбой Кляйзена без шлифов капилляр и термометр вставляют через кусочки резиновой вакуумной трубки, обеспечивающие должную герметичность.
Значительные трудности возникают при перегонке в вакууме пенящихся жидкостей. Чтобы избежать переброса жидкости, рекомендуется заполнять боковое горло колбы или насадки отрезками стеклянных трубок, стеклянной ватой или же вставлять вместо термометра второй стеклянный капилляр. Пенящиеся жидкости перегоняют при незначительном заполнении перегонной колбы. Пенообразование часто вызывается примесями, содержащимися в перегоняемой жидкости; при повторной перегонке пена, как правило, не образуется.
Перегонную колбу обычно нагревают на силиконовой бане - для жидкостей, кипящих ниже 200 °С, или металлической - для высококипящих жидкостей. Температуру бани контролируют термометром. Дистиллят охлаждают так же, как и при перегонке при атмосферном давлении.
Чтобы собирать несколько фракций дистиллята отдельно, не отключая вакуум, пользуются различными устройствами. К наиболее простым из них относится алонж «паук». Отводы «паука» соединяют с приемниками, объем которых соизмеряют с ожидаемым объемом фракции. В качестве приемников применяют круглодонные или остродонные колбочки или пробирки со шлифами; шлифы смазывают чистым касторовым маслом или глицерином. Смазка обеспечивает хорошее скольжение и предотвращает заклинивание шлифов.
Устройство, позволяющее менять любое число приемников во время перегонки, представлено на рис. 162. Пользование подобным приемником для сбора низкокипящих жидкостей исключает возможность контакта паров фракций дистиллята, находящихся в отдельных приемниках, и тем самым предотвращает взаимное загрязнение фракций.

Применение для создания вакуума водоструйного насоса не требует дополнительных приспособлений для поглощения паров перегоняемой жидкости; нужно только предохранять приемник и перегонную колбу от попадания воды, для этого между насосом и прибором перегонки помещают предохранительную склянку. Если используют масляный вакуумный насос, то между перегонным прибором и насосом должна находиться поглотительная или вымораживающая система.
Вакуумная перегонка взрывоопасна. Мелкие осколки стекла, образующиеся при взрыве вакуумированного сосуда, представляют большую опасность, особенно для глаз. Поэтому при проведении работ под вакуумом необходимо надевать защитные очки или пользоваться защитной маской.
Перед началом вакуумной перегонки следует проверить герметичность системы при минимальном давлении без применения нагрева.
Запрещается создавать вакуум в перегонной колбе, наполненной горячей жидкостью. После отгонки растворителя при атмосферном давлении следует сначала охладить содержимое колбы, а затем включить вакуум-насос.
Стеклянные сосуды, например вакуум-эксикаторы, в которых создано уменьшенное давление, должны быть закрыты чехлом или обернуты легкой прочной тканью, чтобы предотвратить разлетание осколков (при взрыве сосуда). Переносить вакуумированные сосуды с места на место не рекомендуется.
При окончании вакуумной перегонки нефтепродуктов включать насос и сообщать систему с воздухом следует, если температура нефтепродукта не менее чем на 50 °С ниже температуры его самовоспламенения.
Перегонку с водяным паром применяют для выделения, очистки и разделения веществ, мало растворимых в воде и обладающих достаточным давлением паров при температуре кипения воды. Если вещества нерастворимы в воде, давление паров смеси равно сумме парциальных давлений паров каждого из компонентов. Вследствие этого температура кипения вещества при перегонке с водой всегда ниже температуры кипения воды при данном давлении. Поэтому перегонка с водяным паром позволяет отгонять вещества, которые при обычной перегонке в той или иной степени разлагаются.
Если вещества растворимы в воде, давление их паров в присутствии воды понижается. Например, масляная кислота, растворяющаяся в воде хуже, чем муравьиная, с водяным паром перегоняется лучше, чем муравьиная, несмотря на то, что температура кипения муравьиной кислоты 101 °С, а масляной - 162°С.
Перегонку с водяным паром можно проводить как при атмосферном давлении, так и в вакууме. Подводимый водяной пар должен быть насыщен или перегрет. Перегретый водяной пар позволяет отгонять вещества с довольно низким давлением паров. Для перегревания водяного пара пользуются пароперегревателями. Они обычно представляют собой металлическую или стеклянную спираль, нагреваемую газовыми горелками или нагревательными банями, в которой насыщенный водяной пар превращается в перегретый.
Перегонка с водяным паром производится на установке, представленной на рис. 163. Колбу располагают наклонно, чтобы летящие вверх брызги не попадали в отводящую пары трубку.

Пар, поступающий из паровика, очень влажен, и перегонная колба может быстро заполниться водой, поэтому между паровиком и перегонной колбой устанавливают водоотделитель.
Для перегонки с водяным паром в вакууме в качестве парообразователя используют перегонную колбу, присоединяя ее к вакуумной линии. Тонкий капилляр, помещенный в колбу, позволяет регулировать расход водяного пара.
В процессе перегонки с водяным паром перегонную колбу следует подогревать, а горло колбы теплоизолировать асбестовым шнуром. Если из холодильника начнут выходить не сконденсировавшиеся пары дистиллята, нужно уменьшить подачу пара или увеличить подачу охлаждающей воды в холодильник.
При перегонке твердые вещества часто затвердевают в холодильнике. Кристаллы целесообразно расплавить в процессе перегонки, прекращая временно подачу охлаждающей воды в холодильник. Если температура плавления твердого вещества выше температуры пара, то по окончании перегонки это вещество выталкивают из холодильника длинной стеклянной палочкой или извлекают подходящим растворителем, из которого оно хорошо кристаллизуется.
При перегонке с водяным паром иногда образуются устойчивые эмульсии. В этом случае перегнанный продукт может быть выделен выслаиванием или экстрагированием органическим растворителем.
О конце перегонки веществ, нерастворимых в воде, судят по отгону прозрачной воды, не содержащей маслянистых примесей. При перегонке веществ, растворимых в воде, о ходе перегонки судят по физическим, химическим или другим свойствам дистиллята.
4.2.1. Общие сведения
Достаточно полное разделение воздуха достигается в результате непрерывной ректификации, которая осуществляться в ректификационных колоннах. Схема такой колонны представлена на рис.4.4.
В нее на разделение подается жидкая бинарная смесь веществ (А+К). В колонне создаются два непрерывных встречных потока: вверх – пары; вниз – жидкость.
В испарителе к жидкой смеси подводится теплота Q и, под воздействием которой жидкость кипит. Пар поднимается по колонне и при этом он обогащается легкокипящим компонентом.
Рис.4.4. Схема ректификационной колонны и процесса ректификации бинарного раствора в ней
Это происходит потому, что верхняя часть колонны холоднее, а нижняя теплее. Таким образом, пар поднимающийся вверх постепенно охлаждается, а жидкость стекающая вниз, постепенно нагревается. За счет разности температур по высоте колонны происходит непрерывный процесс тепломассообмена.
Продукты разделения выводятся из колонны как в жидком, так и парообразном состоянии, как показано на схеме.
Термодинамические основы и принцип работы ректификационной колонны не зависят от температурного уровня проходящих в ней процессов. Т.е. внутренние процессы одинаковы и при Т >Т о.с и Т <Т о.с.
Но во внешних процессах, т.е. в подводе теплоты Q и и отводе Q к есть отличия. Нельзя организовать непосредственный нагрев в испарителе, а также охлаждение в конденсаторе. Так как процесс конденсации происходит при криогенных температурах, то для его организации необходимы циклы криогенного обеспечения. Они требуют значительных затрат энергии. Тем более, что потери при низких температурах всегда выше, чем при высоких.
Например : при подводе в испарителе 1000 кДж теплоты при t и =200°С (473 К) ее ценность (в единицах эксергии) составит
При отводе из конденсатора такого же количества теплоты Q к =1000 кДж при температуре t к =-200°С (73 К), его ценность составит
т.е. примерно в 8 раз больше.
Организовать нагрев в испарителе за счет внешнего теплоподвода просто – достаточно нарушить теплоизоляцию. Но этот путь неприемлем, т.к. эту теплоту затем нужно будет удалять в конденсаторе. И, как мы видели, очень дорогой ценой. Поэтому теплота испарения, обычно, отбирается у самого сжижаемого газа (воздуха).
4.2.2. Колонна однократной ректификации (для получения кислорода)
Это наиболее простое устройство для ректификации воздуха. Для лучшего понимания на рис.4.5 вместе с колонной приведена схема сжижения воздуха по К. Линде, хотя можно применить любую другую схему.

Рис. 4.5. Схема колонны однократной ректификации для получения кислорода в блоке с воздухосжижительной установкой К.Линде
Работа установки в процессах:
1-2 – изотермическое сжатие атмосферного воздуха;
2-3 – охлаждение сжатого воздуха в теплообменнике ТО встречными потоками азота (А), кислорода (К) воздуха (В);
3-4 – сжижение воздуха в змеевике испарителя. Здесь воздух является источником теплоты Q и;
4-5 – дросселирование. Флегма при давлении Р »0,1 МПа подается на верхнюю тарелку колонны;
В т.6 отводятся пары азота, но не чистые, а равновесные кипящему воздуху при температуре Т 5 (в т.5). Поэтому они содержат примерно 10-12 % кислорода. Пары отводятся в ТО, где охлаждают встречный поток сжатого воздуха, идущего в змеевик испарителя для конденсации.
В испарителе колонны скапливается кислород (как более труднокипящая жидкость). Он может отводиться в жидком (в т. 7") или газообразном (в т. 7) виде.
В такой установке можно получить до 2/3 технически чистого кислорода от общего количества кислорода в воздухе переработанного установкой. Около 1/3 теряется с азотом. Давление в колонне близко к атмосферному и не превышает 0,13-0,15 МПа.
4.2.3. Колонна однократной ректификации для получения азота
Особенность этой колонны – наличие конденсатора.

Рис.4.6. Схема колонны однократной ректификации для получения азота:
ТО – теплообменник
Сжатый и охлажденный воздух через дроссельный вентиль подается в куб колонны, при этом происходит его сжижение и частичное испарение. Обогащенный азотом пар по колонне поднимается вверх на встречу стекающей флегме и, уже практически чистый азот, попадает в трубное пространство конденсатора. Здесь азот конденсируется за счет отвода теплоты кипящему обогащенным кислородом жидкому воздуху, который поступает из куба через дроссель Др 2 в межтрубное пространство конденсатора.
Флегма, образующаяся в конденсаторе, по существу чистый азот, стекая вниз по колонне скапливается в карманах конденсатора и отводится как конечный продукт в жидком виде.
Чистые пары азота скапливаются под крышкой конденсатора. Отсюда они отводятся как конечный продукт – газообразный азот.
Обогащенный кислородом воздух из межтрубного пространства конденсатора используется для охлаждения сжатого воздуха в ТО.
4.2.4. Колонна двукратной ректификации
Колонну двукратной ректификации разработал и создал К. Линде в 1907 г. для разделения воздуха. Она позволяет более полно извлекать кислород из воздуха и дает возможность получать не только технически чистый кислород (99,2 % О 2), но и технически чистый азот (99,99 % N 2).
В эту установку составной частью входит колонна однократной ректификации. Аппарат состоит из двух частей (см. рис.4.7): колонны высокого давления (нижняя часть) и колонны низкого давления (верхняя часть).

Рис.4.7. Схема колонны двукратной ректификации с подачей насыщенного воздуха непосредственно в куб
Работа схемы .
Сжатый воздух, охлажденный в теплообменнике (ТО), дросселируется в Др 1 и поступает в куб нижней колонны. При этом он частично сжижается. Обогащенная кислородом жидкость (35-36 % О 2) собирается в нижней части колонны – в кубе. Отсюда она через дроссельный вентиль Др 2 поступает, как исходная жидкость (смесь), в середину верхней части колонны для разделения.
Обогащенный азотом пар в нижней колонне поднимается в трубное пространство конденсатора-испарителя (К-И), где в межтрубном пространстве кипит кислород. Чтобы этот обогащенный азотом пар сконденсировался, надо, чтобы его температура конденсации была выше температуры кипящего кислорода на 2-4 градуса.
Давление в верхней колонне, как и в колонне однократной ректификации, немного выше атмосферного (0,13-0,15 МПа). Температура кипения кислорода при этом будет равна 93-94 К. Следовательно температура азота в нижней колонне должна быть равной 96-97 К. Эта температура может быть температурой конденсации азота при давлении 0,56-0,6 МПа. Именно такое давление устанавливается в нижней колонне.
Жидкий, сконденсировавшийся азот из К-И стекает в нижнюю колонну. Пары поднимаются ему на встречу и обогащаются при этом азотом. Часть жидкого азота скапливается в карманах и в виде флегмы направляется на орошение верхней колонны через ДР 3 . Это позволяет в верхней части колонны получать технически чистый азот.
Таким образом, в результате двойной ректификации воздуха из конденсатора отводится кислород, а из верхней части колонны – азот. После прохождения ТО они являются конечными продуктами.
В установках небольшой производительности удобнее и эффективнее применять колонны двукратной ректификации с подачей воздуха высокого давления через змеевик в кубе (см. рис.4.8).

Рис.4.8. Схема колонны двукратной ректификации с подачей насыщенного сжатого воздуха через змеевик в кубе нижней колонны
В этом змеевике воздух полностью конденсируется и одновременно осуществляется испарение жидкости в испарителе (кубе). Жидкость в кубе обогащается кислородом до 45 % (выше, чем в предыдущей схеме). Это позволяет увеличить флегмовое число (по азоту) в верхней колонне и, следовательно, улучшить показатели установки.
О.С.ГАБРИЕЛЯН,
И.Г.ОСТРОУМОВ,
А.К.АХЛЕБИНИН
СТАРТ В ХИМИЮ
7 класс
Продолжение. Начало см. в № 1, 2, 3, 4, 5, 6, 7, 8, 9/2006
Глава 3.
Явления, происходящие с веществами
(окончание)
§ 17. Дистилляция, или перегонка
Получение дистиллированной воды
Вода из-под крана чиста, прозрачна, не имеет
запаха… Но чистое ли это вещество с точки зрения
химика? Загляните в чайник: в нем легко
обнаруживаются накипь и коричневатый налет,
которые появляются на спирали и стенках чайника
в результате многократного кипячения в нем воды
(рис. 71). А известковый налет на кранах? И
природная, и водопроводная вода – это однородные
смеси, растворы твердых и газообразных веществ.
Конечно, их содержание в воде очень мало, но эти
примеси могут привести не только к образованию
накипи, но и к более серьезным последствиям. Не
случайно лекарства для инъекций готовят только с
использованием специально очищенной воды,
называемой дистиллированной
.
Откуда взялось такое название? Воду и другие жидкости очищают от примесей с помощью процесса, называемого дистилляцией, или перегонкой . Сущность дистилляции состоит в том, что смесь нагревают до кипения, образующиеся пары чистого вещества отводят, охлаждают и вновь превращают в жидкость, которая уже не содержит загрязняющих примесей.
На учительском столе собрана лабораторная установка для перегонки жидкостей (рис. 72).
В перегонную колбу учитель наливает воду, подкрашенную в оранжевый цвет растворимой неорганической солью (дихроматом калия). Так вы воочию убедитесь, что в очищенной воде этого вещества не будет. Для равномерного кипения в колбу бросают 3–4 кусочка пористого фарфора или пемзы (кипелки).
В рубашку холодильника подается вода, а перегонная колба нагревается до кипения содержимого с помощью электронагревателя. Пары воды, попадая в холодильник, конденсируются, и дистиллированная вода стекает в приемник.
Какую температуру показывает термометр? Как вы думаете, через какой отвод в холодильник подается холодная вода, а через какой она сливается?
Дистиллированная вода используется не только для приготовления лекарств, но и для получения растворов, применяемых в химических лабораториях. Даже автомобилисты используют дистиллированную воду, доливая ее в аккумуляторы для поддержания уровня электролита.
А если требуется получить твердое вещество из гомогенного раствора, то используют выпаривание , или кристаллизацию.
Кристаллизация
Один из способов выделения и очистки твердых веществ – кристаллизация. Известно, что при нагревании растворимость вещества в воде увеличивается. Значит, при охлаждении раствора некоторое количество вещества выпадает в виде кристаллов. Проверим это на опыте.
Демонстрационный эксперимент. Помните красивые оранжевые кристаллы дихромата калия, которыми учитель «подкрашивал» воду для дистилляции? Возьмем примерно 30 г этой соли и «загрязним» ее несколькими кристалликами марганцовки. Как очистить основное вещество от внесенной примеси? Смесь растворяют в 50 мл кипящей воды. При охлаждении раствора растворимость дихромата резко понижается, и вещество выделяется в виде кристаллов, которые можно отделить фильтрованием, а затем промыть на фильтре несколькими миллилитрами ледяной воды. Если растворить очищенное вещество в воде, то по цвету раствора можно определить, что марганцовки оно не содержит. Марганцовка осталась в исходном растворе.
Добиться кристаллизации твердого вещества из раствора можно упариванием растворителя. Для этого и предназначены чашки для выпаривания, с которыми вы встречались во время знакомства с химической посудой.
Если испарение жидкости из раствора происходит естественным путем, то для этой цели используют специальные стеклянные толстостенные сосуды, которые так и называются – кристаллизаторы. С ними вы также знакомились в практической работе № 1.
В природе соляные озера – это своеобразные бассейны для кристаллизации. За счет испарения воды на берегах таких озер кристаллизуется гигантское количество соли, которая после очистки попадает к нам на стол.
Перегонка нефти
Дистилляцию используют не только для очистки веществ от примесей, но и для разделения смесей на отдельные порции – фракции, различающиеся температурой кипения. Например, нефть – это природная смесь очень сложного состава. При фракционной перегонке нефти получают жидкие нефтепродукты: бензин, керосин, дизельное топливо, мазут и другие. Процесс этот ведут в специальных аппаратах – ректификационных колоннах (рис. 73). Если в вашем городе есть нефтеперерабатывающий завод, вы могли видеть эти химические аппараты, которые непрерывно разделяют нефть на важные и нужные в жизни современного общества продукты (рис. 74).
Бензин – это основное топливо для легковых автомобилей. Трактора и грузовики используют в качестве такового другой нефтепродукт – дизельное топливо (солярку). Топливом для современных самолетов является главным образом керосин. На этом небольшом примере вы можете понять, насколько важен в современной жизни такой процесс, как перегонка нефти.
 |
Рис. 74.
|
Фракционная перегонка жидкого воздуха
Вы уже знаете, что любые газы смешиваются в любых соотношениях. А можно ли из смеси газов выделить отдельные компоненты? Задача не из простых. Но химики предложили очень эффективное решение. Смесь газов можно превратить в жидкий раствор и подвергнуть его дистилляции. Например, воздух при сильном охлаждении и сжатии сжижают, а затем позволяют один за другим выкипать отдельным компонентам (фракциям), поскольку они имеют различные температуры кипения. Первым из жидкого воздуха испаряется азот (рис. 75), у него самая низкая температура кипения (–196 °С). Затем из жидкой смеси кислорода и аргона можно удалить аргон (–186 °С). Остается практически чистый кислород, который вполне годится для технических целей: газовой сварки, химического производства. А вот для медицинских целей его нужно очищать дополнительно.
Азот, полученный таким способом, используют для производства аммиака, который в свою очередь идет на получение азотных удобрений, лекарственных и взрывчатых веществ, азотной кислоты и т.д.
Благородный газ аргон используют в особом виде сварки, которая так и называется – аргоновая.
1. Что такое дистилляция, или перегонка? На чем она основана?
2. Какая вода называется дистиллированной? Как ее получают? Где она применяется?
3. Какие нефтепродукты получают при перегонке нефти? Где они применяются?
4. Как разделить воздух на отдельные газы?
5. Чем выпаривание (кристаллизация) отличается от перегонки (дистилляции)? На чем основаны оба способа разделения жидких смесей?
6. Чем отличаются процессы выпаривания и кристаллизации? На чем основаны оба способа выделения твердого вещества из раствора?
7. Приведите примеры из повседневной жизни, в которых применяется выпаривание и дистилляция.
8. Какую массу соли можно получить при выпаривании 250 г 5%-го раствора? Какой объем воды можно получить из этого раствора при помощи дистилляции?
ПРАКТИЧЕСКАЯ РАБОТА № 4.
Выращивание кристаллов соли
(домашний эксперимент)
Перед тем как приступить к выполнению работы, внимательно прочитайте ее описание до конца.
Прежде всего выберите подходящую для эксперимента соль. Для выращивания кристаллов подойдет любая хорошо растворимая в воде соль (медный или железный купорос, квасцы и т.д.). Подойдет и поваренная соль – хлорид натрия.
Из оборудования вам понадобятся:
Литровая банка или небольшая кастрюлька, в ней вы будете готовить раствор соли;
Деревянная ложка или палочка для перемешивания;
Воронка с ватой для фильтрования раствора;
Термос с широким горлышком вместимостью 1 л (он нужен для того, чтобы раствор остывал медленно, тогда будут расти крупные кристаллы).
Если нет воронки или нужного термоса, их можно сделать самому.
Чтобы сделать воронку, возьмите пластиковую бутылку из-под напитка и ножницами аккуратно отрежьте ей горлышко, как это показано на рис. 76.
Вместо термоса подойдет обыкновенная стеклянная литровая банка. Поставьте ее в картонную или пенопластовую коробку. Большую коробку брать не нужно, главное, чтобы в нее полностью входила банка. Щели между коробкой и банкой плотно заложите кусочками тряпки или ватой. Чтобы плотно закрыть банку, понадобится пластиковая крышка.
Приготовьте горячий насыщенный раствор соли. Для этого заполните банку наполовину горячей водой (кипяток брать не нужно, чтобы не обжечься). Порциями добавляйте соль и перемешивайте. Когда соль перестанет растворяться, оставьте раствор на одну-две минуты, чтобы нерастворившиеся кристаллы успели осесть. Отфильтруйте горячий раствор через воронку с ватой в чистый термос. Закройте термос крышкой и оставьте раствор медленно остывать два-три часа.
Раствор немного остыл. Теперь внесите в него затравку – кристаллик соли, подвешенный на нитке. После того как ввели затравку, прикройте сосуд крышкой и оставьте на продолжительное время. Чтобы вырос крупный кристалл, потребуется несколько дней или даже недель.
Обычно на нитке вырастает несколько кристаллов. Нужно периодически удалять лишние, чтобы рос один большой кристалл.
Важно записывать условия проведения эксперимента и его результат, в нашем случае это характеристики полученного кристалла. Если получилось несколько кристаллов, то приводят описание самого большого.
Изучите полученный кристалл и ответьте на вопросы.
Сколько дней вы выращивали кристалл?
Какова его форма?
Какого цвета кристалл?
Прозрачный он или нет?
Размеры кристалла: высота, ширина, толщина.
Масса кристалла.
Зарисуйте или сфотографируйте полученный кристалл.
ПРАКТИЧЕСКАЯ РАБОТА № 5.
Очистка поваренной соли
Целью данной работы является очистка поваренной соли, загрязненной речным песком.
Предложенная вам загрязненная поваренная соль представляет собой гетерогенную смесь кристаллов хлорида натрия и песка. Для ее разделения необходимо воспользоваться различием в свойствах компонентов смеси, например различной растворимостью в воде. Как известно, поваренная соль растворяется в воде хорошо, в то время как песок в ней практически нерастворим.
В химический стакан поместите выданную учителем загрязненную соль и налейте 50–70 мл дистиллированной воды. Перемешивая содержимое стеклянной палочкой, добейтесь полного растворения соли в воде.
Раствор соли от песка можно отделить фильтрованием. Для этого соберите установку как показано на рис. 77. С помощью стеклянной палочки осторожно перелейте содержимое стакана на фильтр. Прозрачный фильтрат будет стекать в чистый стакан, нерастворимые компоненты исходной смеси останутся на фильтре.
Жидкость в стакане – это водный раствор поваренной соли. Выделить из него чистую соль можно выпариванием. Для этого 5–7 мл фильтрата налейте в фарфоровую чашку, поместите чашку в кольцо штатива и осторожно нагревайте на пламени спиртовки, постоянно перемешивая содержимое стеклянной палочкой.
Сравните кристаллы соли, полученные после выпаривания раствора, с исходной загрязненной солью. Перечислите, какие приемы и операции вы использовали для очистки загрязненной соли.